Sabun hemen her evde yer alan sıradan bir tüketim ürünüdür. Ancak her gün milyarlarca insan sabun kullansa da, çoğumuz onun nasıl işlediğini tam olarak bilmeyiz. Bu yazıda sabunun arkasındaki kimyayı inceleyelim ve sabunun kiri nasıl temizlediğini anlamaya çalışalım.

Sabunun kökeni yaklaşık 5.000 yıl öncesine, antik Babil’e kadar uzanıyor. Sabuna dair ilk yazılı kaynaklardan biri Romalı doğa tarihçisi Yaşlı Plinius’un MS 77 tarihli “Naturalis Historia” adlı eseridir. Plinius, sabunu genellikle içyağı ve kül karışımı olarak tanımlar.
Ancak bu sabunlar, kişisel hijyen için değil, daha çok tekstil üretiminde yün ve pamuk gibi lifleri temizlemek amacıyla kullanılıyordu. Hamam kültürüyle tanınan Yunanlılar ve Romalılar bile sabun yerine zeytinyağı kullanır, ardından bir kazıyıcıyla vücutlarını temizlerdi.

.
Orta Çağ’a gelindiğinde sabun Avrupa’da daha yaygın hale geldi. Bitkisel yağ bazlı sabunlar hem daha nazik hem de daha hoş kokulu olduğundan, Avrupa’daki soylular arasında lüks bir tüketim ürünü olarak görülmeye başlandı. İlk örneklerinden biri Halep sabunuydu.
Zeytinyağı ve defne yağı içeren bu sabun, Suriye’de üretildi ve Hristiyan Haçlılar aracılığıyla Avrupa’ya taşındı. Ardından İtalyan, Fransız ve İspanyol versiyonları ortaya çıktı. Özellikle İspanya’nın Kastilya bölgesinde yapılan “Castile sabunu”, Avrupa aristokrasisinin favori temizlik ürünlerinden biri oldu.

Zamanla sabun yalnızca lüks bir eşya olmaktan çıkıp gündelik yaşamın bir parçası haline geldi. 1791’de Fransız kimyager Nicolas Leblanc, ilk sabun üretim sürecini patentledi.
Sabun Kiri Nasıl Temizler?
Su – bilimsel adıyla dihidrojen monoksit – iki hidrojen ve bir oksijen atomundan oluşur. Bu molekül, gezegenimizdeki tüm yaşam için gereklidir. Kimyagerler, suya çekim duyan molekülleri “hidrofilik”, yani “su seven” olarak tanımlar. Hidrofilik moleküller suda çözünür. Bu nedenle, sadece suyla ellerinizi yıkarsanız, cildinize yapışan hidrofilik kalıntıların büyük kısmını uzaklaştırabilirsiniz.
Ancak kimyasal açıdan başka bir molekül sınıfı daha vardır: “hidrofobik”, yani “sudan korkan” moleküller. Bu tür moleküller suda çözünmez. Yağ, bu tür maddelere örnektir. Günlük hayattan da bildiğiniz gibi, yağ ve su birbirine karışmaz. Örneğin bir kavanozda salata sosunu çalkaladığınızda, yağ ve su bazlı içerikler bir süre sonra yeniden ayrılır.
Bu nedenle, ellerinizi yalnızca suyla yıkamak, yağ veya gres gibi hidrofobik maddeleri temizlemek için yeterli olmaz. Tam da burada sabun devreye girer.
Sabun molekülü karmaşık bir yapıya sahiptir ve aynı anda hem su seven hem de sudan kaçan özellikler taşır. Şekil olarak kurbağa yavrusuna benzer: Yuvarlak baş kısmı hidrofiliktir; uzun kuyruk kısmı ise hidrofobiktir. Bu özellik sabunun kaygan olmasını sağlar. Aynı zamanda, sabunun temizlikte bu kadar etkili olmasının temel nedeni de budur.
Ellerimizi sabun ve suyla yıkadığımızda neler olur?
Gün boyunca dokunduğumuz her şeyden ellerimize çeşitli kalıntılar bulaşır. Bu kalıntılar, yediğimiz yiyeceklerin izleri, dışarıdan gelen çamur, ter ya da cildimizin salgıladığı doğal yağlar olabilir.
Bu maddeler moleküler düzeyde ya suyu sever (hidrofilik) ya da sudan kaçar (hidrofobik). Yani kir, bu iki tür molekülün karışımıdır. Örneğin toz ve ölü deri hücreleri suyla çözünür; bunlar hidrofiliktir. Vücuttan salgılanan doğal yağlar ise hidrofobiktir. Dış çevreden gelen kir parçacıkları ise her iki özellikten birini taşıyabilir.

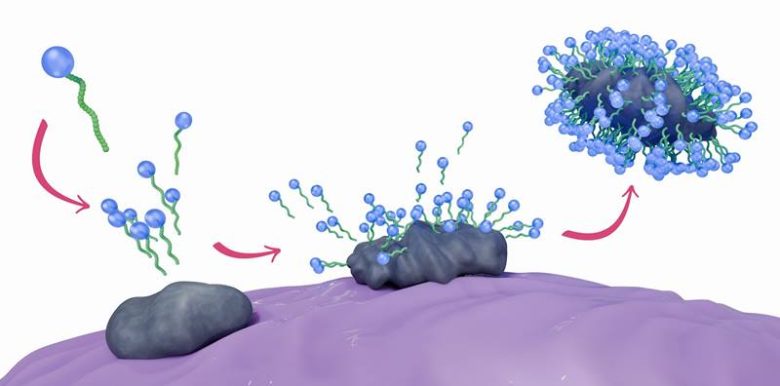
Yalnızca suyla ellerinizi yıkadığınızda, suyu seven molekülleri uzaklaştırabilirsiniz. Ama yağ gibi suyu sevmeyen maddeler ciltte kalır. Sabun hem suyu seven hem de sudan kaçan özelliklere sahip olduğu için, hem hidrofilik hem de hidrofobik kirleri etkili şekilde temizler. Sabun molekülleri bir araya gelerek kirli parçacıkları çevreler. Bu yapıya “misel” denir.
Moleküler düzeyde bakıldığında, sabun molekülleri kirin etrafında bir küre oluşturur: dışta suyu seven başlar, içte suyu sevmeyen kuyruklar yer alır. Böylece kir sabunun içine hapsolur. Sonrasında, akan su bu misel yapısını ve içindeki kirleri cildinizden alıp götürür.
Bu temizlik etkisinin tam olması için, ellerinizi en az 20 saniye boyunca sabunla ovalayarak yıkamanız gerekir. Elleri birbirine sürtmek, sabun moleküllerinin kirlere temas etmesini ve onları parçalayarak sarmasını sağlar.
Kirle birlikte, ellerimizde mikroorganizmalar da bulunur: bakteri, virüs ve mantarlar. Çoğu zararsızdır, hatta bazıları bizi hastalıklardan korur. Ancak “patojen” olarak bilinen bazı mikroorganizmalar hastalıklara yol açabilir. Bu mikroorganizmalar, onları koruyan bir zarla çevrilidir. Sabun ve su bu zarı bozarak yapıyı parçalar. Mikroorganizma yok olur. Akan su ise geride kalan kalıntıları ve kokuları temizler.
Sonuç olarak
“Sabun medeniyetin gidişatını değiştirdi” demek bile aslında yetersiz kalır. Binlerce yıldır milyarlarca insanın sağlıklı kalmasına yardımcı oldu. Bu yüzden, bir dahaki sefere biri size ellerinizi yıkamanızı söylediğinde, sabunun bu etkileyici gücünü hatırlayın.
Kaynaklar ve ileri okumalar:
- Konkol, Kristine & Rasmussen, Seth. (2015). An Ancient Cleanser: Soap Production and Use in Antiquity. 10.1021/bk-2015-1211.ch009.
- Petruzzello, Melissa. “How Does Soap Work?”. Encyclopedia Britannica, 10 Mar. 2022, https://www.britannica.com/story/how-does-soap-work. Accessed 14 July 2024.
- The dirty history of soap. Yayınlanma tarihi: 12 Mayıs 2020. Kaynak site: Conversation. Bağlantı: The dirty history of soap
Size Bir Mesajımız Var!
Matematiksel, matematiğe karşı duyulan önyargıyı azaltmak ve ilgiyi arttırmak amacıyla kurulmuş bir platformdur. Sitemizde, öncelikli olarak matematik ile ilgili yazılar yer almaktadır. Ancak bilimin bütünsel yapısı itibari ile diğer bilim dalları ile ilgili konular da ilerleyen yıllarda sitemize dahil edilmiştir. Bu sitenin tek kazancı sizlere göstermek zorunda kaldığımız reklamlardır. Yüksek okunurluk düzeyine sahip bir web sitesi barındırmak ne yazık ki günümüzde oldukça masraflıdır. Bu konuda bizi anlayacağınızı umuyoruz. Ayrıca yazımızı paylaşarak da büyümemize destek olabilirsiniz. Matematik ile kalalım, bilim ile kalalım.
Matematiksel



