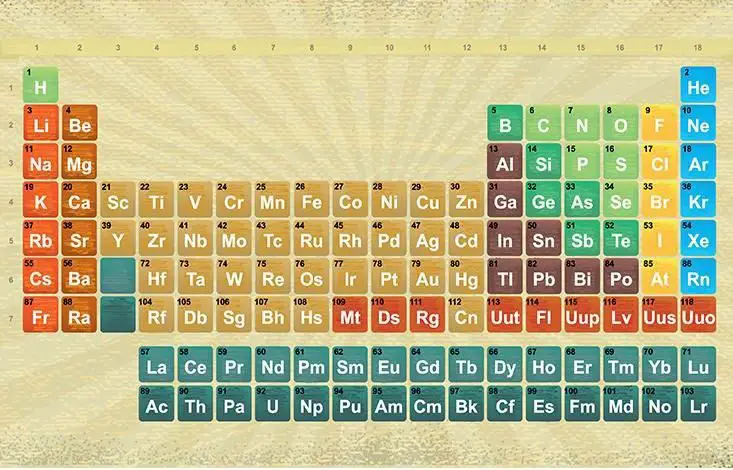
2015 yılının Aralık ayına kadar, periyodik tabloda bazı boşluklar vardı. Neyse ki 113, 115, 117 ve 118. elementlerin yani Nihonium, Moscovium, Tennessine ve Oganesson’un bulunuşu ile boşluklar doldu. Yeni bir sıra başlatacak olan 119 ve 120 elementlerini bulma çalışmaları çoktan başladı. Fakat tam olarak kaç tane daha element olmalı? Periyodik tablonun sonuna ne zaman geleceğiz?
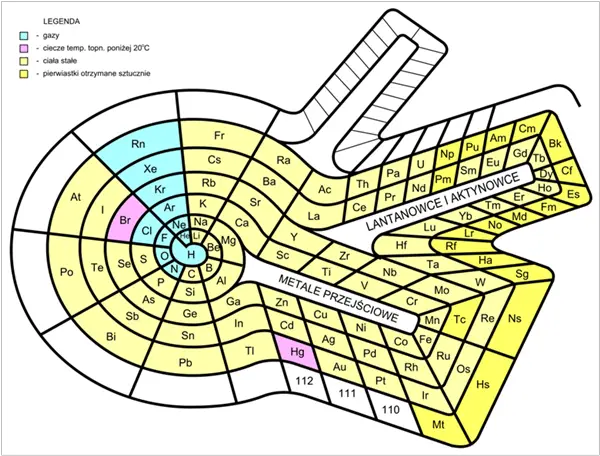
Periyodik tabloda bulunan elementlerin her biri belirli parametreler göz önüne alınarak bugün bulundukları yerlerde bulunmaktadır. Bununla birlikte periyodik tablonun düzeni, başlangıcından bu yana zamanla değişti. Bunun nedeni elbette süreç içinde yeni elementlerin keşfedilmesi ve periyodik tabloya eklenmesiydi.

Mendeleyev’in tablosu yayınlandığında atom altı parçacıklar henüz bulunmamıştı. Bu yüzden hazırladığı tablo tam olarak doğru olmayacaktı. Fakat onun çalışmasının en önemli özelliği, elementlerin atom ağırlıkları ile fiziksel ve kimyasal özellikleri arasında bağ olduğunu ortaya koymasıydı.
Mendeleyev, periyodik tablonun bu ilk haliyle bilinmeyen elementlerin keşfinin başlamasına sebep olmuş ve elementlerin özelliklerinin daha iyi anlaşılacağı yeni bir döneme ışık tutmuştu.

Modern Periyodik Tablonun Sorunları
150 yıl içinde maddeyi anlamamızda birçok değişiklikler oldu. Protonların keşfedilmesinden sonra bilim insanları bir elementin atom sayısının çekirdeğindeki proton sayısına eşit olduğunu gördüler. Bu yüzden modern periyodik tabloda elementler atom kütlesine göre değil atom sayısına göre diziliyor. Elementlerin özelliklerinde tekrar eden şablonlar var bu yüzden tabloya periyodik ismi veriliyor.
Modern periyodik tablo, protonlar ve elektronlar gibi atom altı parçacıkların davranışını açıklamak için 20. yüzyılda ortaya çıkan kuantum fiziği ile aşağı yukarı tutarlıydı. 1981’deki keşfinden sonra 107. element olan Bohrium, onu çevreleyen diğer geçiş metallerine son derece düzgün uyuyordu.
Bu nedenle onu keşfeden araştırmacılardan biri “bohrium sıkıcı (bohrium is boring)” diyerek bunun ne kadar öngörülebilir olduğunu belirtmişti. Ancak önümüzdeki süreç daha ilginç olacak gibi gözüküyor.

Örneğin, kendi gruplarının diğer üyeleriyle lutesyum ve lavrensiyumdan daha az ortaklığa sahip olan lantan ve aktinyum ile ilgili henüz çözümlememiş bir sorun var. 2. element olan helyum bile bazı noktalarda sorunlara yol açıyor. Periyodik tablonun alternatif bir versiyonu helyumu en dıştaki elektronları yerine tüm elektronlarının düzenine dayanarak berilyum ve magnezyum ile aynı sıraya koyuyor.
Görelilik Teorisi İle İlgili Sorun Var
Einstein’ın, Mendeleev’in tablosundan on yıllar sonra yayınlanan, özel görelilik teorisi de sistemde bazı çatlaklar olduğunu ortaya çıkarmış durumda. Görelilik, bir parçacığın kütlesinin hızı ile arttığını belirtir. Bu, bir atomun pozitif yüklü çekirdeğinin etrafında dönen negatif yüklü elektronların tuhaf davranmasına ve elementin özelliklerini etkilemesine neden olabilir.
Mesela altın elementini düşünün. Çekirdek 79 pozitif protonla doludur. Bu nedenle içe doğru düşmemek için elektronlar ışık hızının yarısından daha fazla hızda dolaşmak zorundadır. Bu onları daha büyük hale getirdiği gibi daha sıkı, daha düşük enerjili bir yörüngeye de çeker. Bu konfigürasyonda, elektronlar mavi ışığı yansıtmak yerine emer ve alyanslara kendilerine özgü bir ışıltı verir.
Ünlü fizikçi Richard Feynman’ın, görelilik yardımıyla, periyodik tablonun sonunun 137. element olacağını tahmin ettiği söylenir. Feynman için, 137 “sihirli bir sayı” dır. Bu sayı fiziğin başka bir yerinde herhangi bir neden olmadan ortaya çıkmıştır. Detaylar için: Neden 137 Sayısı Fizikteki En Büyük Gizemlerden Birisidir?
Hesaplamaları, 137’nin ötesindeki elementlerdeki elektronların ışık hızından daha hızlı hareket etmesi ve böylece çekirdeğe çarpmamak için görelilik kurallarını ihlal etmesi gerektiğini gösterir. O zamandan beri daha yeni hesaplamalar bu limiti aştı.
Periyodik Tablo İle İlgili Birkaç İlginç Bilgi

Periyodik tablodaki elementlerden birisi adını İskandinav Mitolojisindeki tanrılardan alır. Toryum doğada oluşan radyoaktif bir metal. Sembolü ise Th. Atom numarası ise 90. Bu elemente İskandinav mitolojisindeki Şimşekler tanrısı Thor’un adını verdi.
Şu anda bir elemente ismini vermiş olan ve hâlâ hayatta olan tek bir bilim insanı var. Rus bilim insanı Yuri Oganessian’ın takma adı ‘Bay Element 118’. Sembolü Og olan sentetik radyoaktif element Oganesson’un isim babası.
Sadece iki element kadınların ismini taşıyor. Sembolü Cm ve atom numarası da 96 olan Küryum’un adı Marie ve Pierre Curie’den geliyor. Meitneryum ise nükleer fisyon alanındaki çalışmalarıyla bilinen kadın fizikçi Lise Meitner’in adını taşıyor.
İskandinavya’da bir kentin yakınlarındaki bir köy, dört elemente birden ismini verdi. Stokholm yakınlarındaki Ytterby, periyodik tabloda adından sıkça söz ettiriyor. Kimyasal elementler Yttryum, Terbiyum, Erbiyum ve Ytterbiyum köy yakınlarındaki bir madende keşfedilmişlerdi.
Kaynak; When Will We Reach the End of the Periodic Table?; https://www.smithsonianmag.com
Matematiksel










