Buhar makinesi dünyayı modernleştirmeye başladığından beri termodinamiğin ikinci yasası ve beraberinde entropi kavramı fizik, kimya, mühendislik ve biyoloji üzerindeki hükmüne devam ediyor. Peki entropi tam olarak nedir?

Hayatın devamı, düzenin korunmasına bağlıdır. Vücudumuz, doğru koşullar sağlanmadığında veya yeterince beslenmediğinde ölür. Elektronik eşyalar, kabloları karıştırıldığında bozulur. Yatağımızı toplamadığımızda ailemiz hayal kırıklığına uğrar. Her şeyin çalışması için bir tür düzenin, yapının korunması gerekir.
Ancak ne kadar uğraşırsak uğraşalım, evren sanki dağınıklığı destekliyor gibidir. Bu durumu tanımlayan bir kavram var: entropi. Ve fiziğe göre entropiye karşı kazanma şansımız yok. İkinci termodinamik yasası der ki: Evrenin toplam entropisi ya sabit kalır ya da artar.

Başka bir deyişle, düzensizlik zamanla mutlaka büyür. Belki de düzen dediğimiz şey, aslında sadece kaosun istisnasıdır. Gezegenimiz, bedenlerimiz ve yaptığımız her şey, yasaya uyumlu, boş bir evrende sadece küçük bir sapmadır.
Entropiyi açıklamanın en yaygın yolu, onu düzensizlik ya da rastlantısallık olarak tanımlamaktır. Örneğin, tertemiz bir oda, iki hafta boyunca toparlanmamış haline göre daha düşük entropiye sahiptir. Zamanla daha dağınık hale gelir, ama ne yazık ki, kendiliğinden tekrar tertemiz olması pek mümkün değildir.
Bu da bize entropinin basit ama etkili bir kuralını hatırlatır: Düzenli sistemler zamanla düzensizliğe yönelir. Entropi nedir? sorusuna cevap arıyorsanız öncelikler termodinamik yasalarını bilmeniz gerekir.
Termodinamik Yasaları Nelerdir?
Bir fincan sıcak çayı masanın üstünde bıraktığınızda, ya da bir nesneyi daha serin bir ortamda unuttuğunuzda, bu nesnelerin zamanla soğuması kaçınılmazdır. Ancak bu sürecin nasıl işlediğini bize açıkça anlatan şey termodinamik bilimidir.
Termodinamik; ısı, iş, sıcaklık ve enerji arasındaki ilişkileri inceler. Basitçe söylemek gerekirse, enerjinin bir yerden başka bir yere ve bir biçimden başka bir biçime nasıl aktarıldığını açıklar. Klasik termodinamik yalnızca birkaç temel yasaya dayanır. Bu yasaların numaralandırması biraz gariptir: sıfırdan başlar ve üçte sona erer. Entropi kavramı ise, bu temel yasalar arasında özel bir yer tutar.
Termodinamiğin Sıfırıncı Yasası Nedir?
Sıfırıncı yasa,, birinci ve ikinci yasalar zaten çoktan yerleşmişken, 1931 yılında Ralph H. Fowler tarafından ortaya atılmış ve geriye dönük olarak “sıfırıncı” olarak adlandırılmıştır.
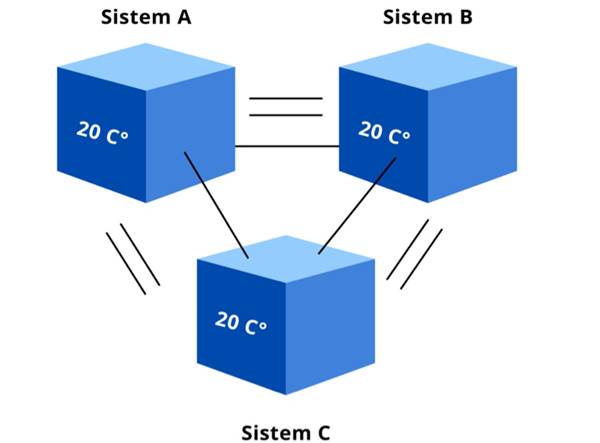
Sıfırıncı yasa, sistemlerin hangi koşullarda mekanik denge veya daha spesifik olarak termal denge durumunda olacağını anlamamıza olanak sağlar. Üç sistemden ikisi ayrı ayrı üçüncü bir sistemle termal dengede ise, bu iki sistem de birbiriyle termal dengededir. Bu ortak durumu tanımlayan fiziksel büyüklüğe ise sıcaklık adı verilir. Özetle: Sıfırıncı yasa, sıcaklık kavramının temelini oluşturur.
Termodinamiğin Birinci Yasası Nedir?
Termodinamiğin Birinci Yasası aslında bildiğimiz bir şeyi söyler: Enerji yoktan var edilemez, vardan yok edilemez. Sadece bir halden başka bir hale dönüşür. Örneğin ısı elektrik enerjisine çevrilebilir, ama sıfırdan enerji yaratamayız. Aynı şekilde, enerji kendi kendine ortadan kaybolamaz. Bir sistem enerji kazanıyorsa, o enerji mutlaka başka bir yerden gelmek zorundadır.
Bu yasa şunu ifade eder: Bir sistemin iç enerjisindeki değişim, dışarıdan verilen ısı miktarı ile sistemin yaptığı iş arasındaki farka eşittir. Kısacası, her şeyin çalışabilmesi için bir enerji kaynağına ihtiyacı vardır.
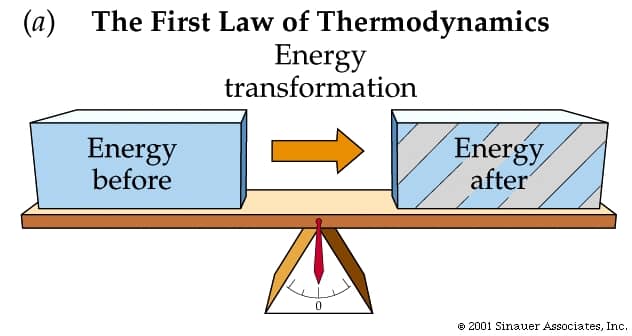
Sıfırıncı ve Birinci Yasa, termodinamiğin temel taşlarını oluşturur. Sıfırıncı yasa sıcaklık kavramını tanımlar. Birinci yasa ise enerjinin nasıl korunup aktarıldığını anlatır. İkinci yasa ise bambaşka bir kavramı, yani entropiyi karşımıza çıkarır.
Termodinamiğin İkinci Yasası ve Entropi Nedir?
Termodinamiğin ikinci yasası, istatistiksel ilkeleri kullanarak çok sayıda nesnenin davranışını tanımlayan istatistiksel mekanik alanından gelir. Bunun yararlı olduğu bariz bir yer, gazların veya sıvıların davranışıdır. İkinci Yasa, termodinamik süreçlerin, yani ısı enerjisinin transferini veya dönüşümünü içeren süreçlerin geri döndürülemez olduğunu belirtir çünkü hepsi entropide artışa neden olur.
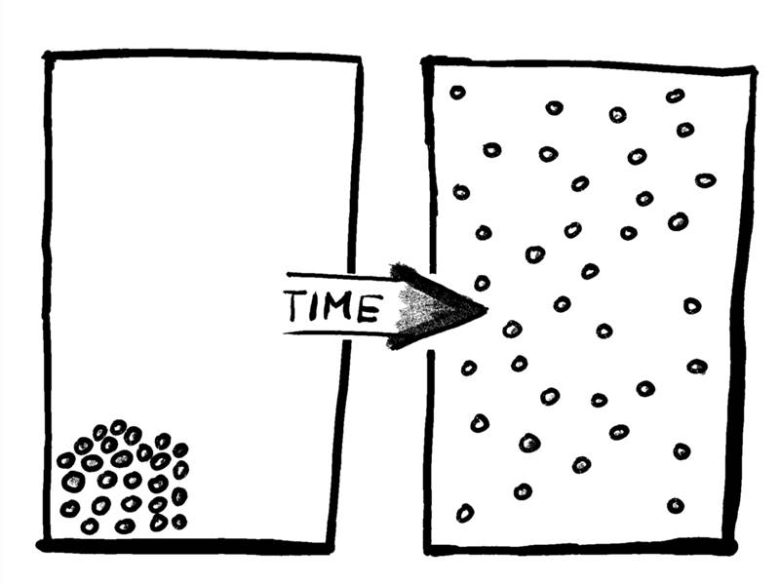
Düzensizlik doğası gereği basittir. Daha az bilgi gerektirir, daha az enerji taşır ve her şeyin birbirine karıştığı, farkların ortadan kalktığı bir duruma yönelir. Doğa da tam olarak bunu sever.
Bir bardak buz, bir bardak sudan çok daha düzenlidir. Buzun molekülleri belirli bir kafes yapısında sabitlenmiştir. Bu düzeni tarif etmek için her molekülün yerini, yönünü ve birbirine olan mesafesini tek tek tanımlamanız gerekir. Oysa bir bardak suyu tarif etmek için sadece bardağın şekli ve suyun seviyesi yeterlidir. Çünkü sıvı moleküller sürekli, rastgele hareket eder. Bu yüzden buz, sudan çok daha karmaşıktır ve istatistiksel olarak daha az olasıdır.
Entropi, enerjiyi de daha düşük ve dengeli bir seviyeye sürükler. Çünkü doğada kendiliğinden oluşan süreçler, her zaman dengesizlikleri azaltır. Yarım bardak buz ve yarım bardak kaynar su, içinde büyük bir sıcaklık farkı barındırır ve bu düşük entropili bir durumdur. Ancak zamanla buz erir, sıcaklıklar eşitlenir ve ortaya ılık bir su çıkar. Denge artar, enerji eşit dağılır ve sistemin entropisi yükselir. Doğanın yasası budur: Farklar azalır, karışıklık artar ve her şey daha olası olana doğru evrilir.
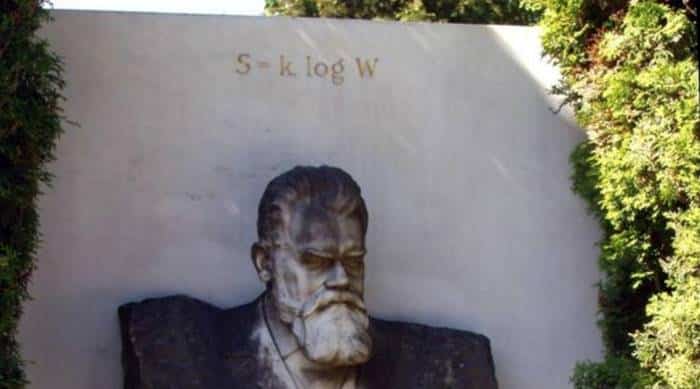
Entropinin matematiksel formülü Ludwig Boltzmann’ın mezar taşında yer almaktadır. Entropide olan değişiklik ΔS biçiminde gösterilirse kısa ve öz bir temsili şu şekilde olur: ΔS ≥ 0
Termodinamiğin Üçüncü Yasası
Doğada her şeyin doğal hali entropinin artmasıdır. Bu yüzden karmaşık sistemler zamanla çözülür, düzensizliğe sürüklenir. İşte bu özellik, fiziksel kavramlar içinde zamanı belirli bir yönde zorunlu kılan nadir gerçeklerden biridir.

Teknik olarak, yanan bir odun parçasının yeniden birleşip eski haline dönmesini veya bir su birikintisinin kendiliğinden donarak ilk haline gelmesini yasaklayan doğrudan bir fizik yasası yoktur — tek engel entropidir. Termodinamiğin üçüncü yasası da, bir sistemin özelliklerini ve entropinin mutlak sıfır olarak bilinen benzersiz bir ortamdaki davranışını tahmin eder.
Termodinamiğin Üçüncü Yasası, bir sistemin sıcaklığı mutlak sıfıra yaklaştıkça entropisinin sabit hale geldiğini veya entropide artık bir değişim yaşanmadığını söyler. Bu yasa, günlük hayatımızda doğrudan karşılaştığımız bir durum değildir. Daha çok bilinen en düşük sıcaklıklarda, nesnelerin davranışlarını ve enerji düzenlerini açıklamak için önem taşır.
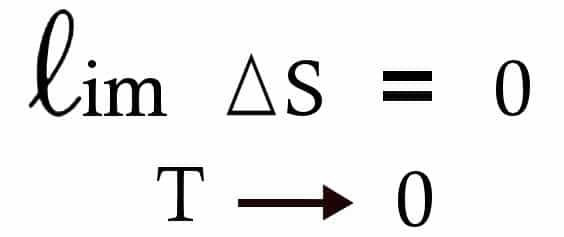
Sonuç olarak
Sonuç olarak, termodinamik ve özelinde entropi oldukça karmaşık bir konudur. Tanımı, uygulandığı sisteme bağlıdır; bu yüzden farklı akademik alanlar, bu kavramın farklı yönlerine odaklanır. Yine de entropi kesinlikle büyüleyici bir konudur. Odanızın dağılmasına neden olan şeyin, bir gün evrenin sonunu getirecek olan aynı ilke olması insanı biraz olsun alçakgönüllü yapıyor.
İngiliz astrofizikçi Arthur Eddington’ın 1920’lerde termodinamiğin “doğa yasaları arasında en üstün konumda” olduğunu şu cümlelerle ifade etmişti. “Teorinizin termodinamiğin ikinci yasasına aykırı olduğu bulunursa size hiçbir umut veremem.”
Kaynaklar ve İleri Okumalar:
- Maths in a minute: The second law of thermodynamics. Yayınlanma tarihi: 2 Haziran 2016; Kaynak site: Plus Math. Bağlantı: Maths in a minute: The second law of thermodynamics/
- Kostic MM. The Second Law and Entropy Misconceptions Demystified. Entropy (Basel). 2020 Jun 11;22(6):648. doi: 10.3390/e22060648. PMID: 33286420; PMCID: PMC7517180.
- What is entropy, and why is it always increasing? Yayınlanma tarihi: 2 Ocak 2021; Kaynak site: ZME. Science. Bağlantı: What is entropy, and why is it always increasing
- Physicists Rewrite the Fundamental Law That Leads to Disorder. Yayınlanma tarihi: 26 Mayıs 2022. Kaynak site: Quanta. Bağlantı: Physicists Rewrite the Fundamental Law That Leads to Disorder
Matematiksel




yazınız , ayrıntıdan uzak olmuş ve gayet anlaşılabilir olmuş.teşekkürler.